Recuperación de la espermatogénesis, conteo y mobilidad optimos
La espermatogénesis es un proceso bien definido, complejo, largo y muy ordenado de división y diferenciación celular, que se encuentra bajo regulación de señales endocrinas (GnRH, LH, Inhibina y FSH); paracrinas, derivadas de la interrelación entre los distintos tipos de células de los túbulos y del intersticio (incluso vía yuxtacrina); y de señales autocrinas, de autocomunicación de una célula consigo misma.
En todo este proceso la testosterona juega un papel fundamental. La testosterona en el interior del túbulo testicular alcanza concentraciones 100 veces mayores que la testosterona circulante en torrente sanguíneo.
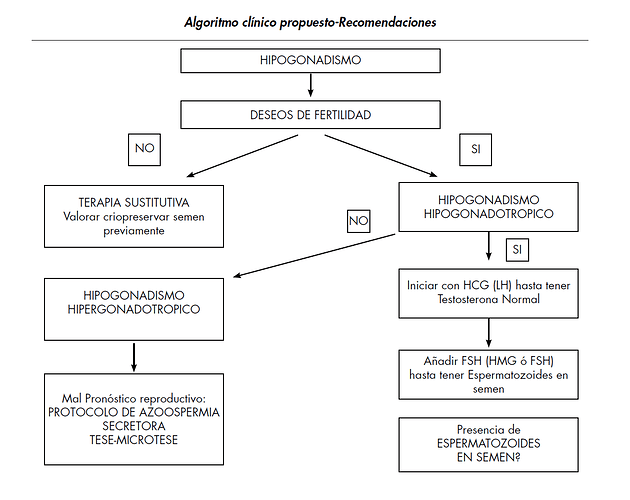
Cuando la prioridad clínica del paciente es la fertilidad, en pacientes con hipogonadismo hipogonadotropo, el tratamiento para restaurar una espermatogenesis normal requiere la administración exógena de gonadotropinas. El tener unos valores mínimos de testosterona que garanticen una espermatogénesis efectiva pueden venir de la administración exógena o de la estimulación endógena testicular con gonadotropinas.
El tratamiento debe ser prolongado, con una duración de al menos 12-18 meses. En el 95% de los casos se va a obtener una respuesta favorable, entendiendo como tal la aparición de espermatozoides en el eyaculado, consecuencia del restablecimiento de la espermatogénesis.
- Pruebas a realizarse previo comienzo de terapia: seminograma, estudio sérico de gonadotropinas y valores hormonales (DHT, TTotal, TLibre, E2…) y si procede volumen testicular para considerar el nivel de atrofia testicular. Estas pruebas se mediran en función de la terapia a realizar.
En el caso de promover una correcta espermatogénesis mediante la estimulación de testosterona endógena (trás el correspondiente PCT): La determinación de gonadotrofinas séricas(FSH y LH) nos diferenciará entre los de origen testicular primario (hipergonadotrópicos) y los secundarios a un trastorno del eje hipotálamo-hipofisario (hipogonadotropicos).
Lo primero es ver de donde partimos, si tenemos un hipogonadismo primario o secundario; ante el primario los niveles de LH Y FSH son normales y debemos estimular primero la produción endogena en los testiculos mediante el uso de LH o HCG. Dividimos el tratamiento en dos fases claramente diferenciadas:
• La primera mediante administración de HCG (con actividad semejante a la LH) a dosis de 1500 UI IM
3 veces por semana hasta alcanzar unos valores normales de testosterona.
• La segunda añadiendo FSH recombinante a dosis de 150 UI IM 3 veces a la semana. Realizando seminogramas hasta lograr recuperar espermatozoides del eyaculado. Aquí se pueden criopreservar.
En el caso de estar en TRT se puede pasar pasar directamente a la segunda fase y añadir FSH.
Si el hipogonadismo es secundario habria que estimular la producción de gonadotropinas a nivel hipotalamo-hipofisiario con clomifeno o cualquier otro SERM en caso de que el clomifeno produciera una inhibición del eje. Hay casos en los que se debe administrar Gnrh para estimular la producción de gonadotropinas en un hipotalamo inhibido.
Regulación testicular
• Células de Sertoli
La testosterona en el interior del túbulo testicular alcanza concentraciones 100 veces mayores que la testosterona circulante en torrente sanguíneo.
Esto se logra gracias a que las células de Sertoli producen la proteína trasportadora de andrógenos
(ABP), una sustancia capaz de unirse a testosterona y DHT con gran afinidad. La ABP actúa como transportadora a través de la barrera hematotesticular e introduce en el interior del túbulo seminífero las grandes cantidades de testosterona necesarias para la espermatogénesis.
La ABP es el análogo intratesticular de la proteína plasmática SHBG. Para la síntesis inicial de la ABP es necesaria la presencia de FSH, pero el nivel puede mantenerse por las altas concentraciones de andrógenos alcanzadas tras la inducción. Este mecanismo permite mantener altas concentraciones
locales de testosterona en el túbulo seminífero y en el epidídimo, estabilizando las fluctuaciones de la secreción de esta hormona por las células de Leydig. El complejo ABP-DHT actúa incrementando la eficacia del proceso meiótico, estimulando los últimos pasos de la maduración de la espermátide e interviniendo, aunque menos, en la fase proliferativa del desarrollode las espermatogonias. No deja de ser curioso que la testosterona, responsable de la espermatogénesis, actúe de forma indirecta sobre las células germinales ya que éstas no poseen receptores androgénicos, mientras que si los presentan las células de Sertoli, de Leydig, mioides peritubulares y de arteriolas.
Hay evidencias de que los andrógenos en las células germinales actúan mediante acción no genómica. La testosterona provoca respuestas a través de mensajeros secundarios, tales como el AMPc, y señalizando rutas diferentes a la transcripción clásica mediada por los receptores androgénicos.
• Células de Leydig, mioides y de Sertoli
Las células mioides, responsables de la contractibidad del tubo seminífero sintetizan, bajo la acción de la testosterona, la proteína moduladora de la célula de Sertoli (P-Mod-S), cuyo papel es de mediadora entre el estroma y el epitelio germinal, regulando a nivel local la espermatogénesis.
La regulación de expresión génica en células germinales masculinas ocurre primero en el nivel de transcripción, después en el nivel de traducción, y a partir de entonces en el nivel post-translación.
Y transcurre en tres niveles concentricos: una regulación intrínseca de las propias células germinales,
una regulación interactiva entre células germinales y vecinas, y una regulación extrínseca modulada por hormonas esteroideas.
En la regulación extrínsecalas hormonas esteroideas (andrógenos y estrógenos) y sus receptores,
actúan a través de tres rutas:
a) Activación directa de genes mediante factores de transcripción, cuya
actividad es hormono-dependiente.
b) Respuesta transcripcional secundaria a través de la activación
de factores transcriptores hormono-dependientes y
c) Respuesta transcripcional independiente (no clásica) a la inducción hormonal.
Por último, en los últimos años, el incremento de estudios sobre la apoptosis, tanto en modelos
con roedores como con ratones mutantes (knock-out) han permitido conocer el papel de las hormonas FSH y Testosterona en estos procesos de apoptosis; Más como factores de supervivencia en la regulación de la ruta específica de genes y proteínas apoptóticos, que en la proliferación.
La FSH y la testosterona presentan acciones antiapoptóticas e inhibitorias. Así, bajo cultivo, en ausencia de suero y testosterona, las tasas de apoptosis en los túbulos seminíferos humanos aparecen incrementadas. La adición de testosterona inhibió la apoptosis de las células de Sertoli, potenció la acción estimuladora de la FSH en las células germinales premeióticas y estimuló la espermiogénesis, mientras que la FSH inhibió la diferenciación de espermátida.
La FSH estimula la espermiogénesis temprana (espermátidas redondas tempranas a espermátidas
redondas tardías) y espermiogénesis media (espermátidas redondas tardías a espermátidas elongándose tempranas). Por el contrario, la testosterona potencia los efectos de la FSH en la espermiogénesis temprana y media, y estimula los pasos finales de la maduración espermiogenica.
Tratamiento del hipogonadismo hipogonadotropo
Existen distintas formas de administración:
• Administración de HCG (con actividad semejante a la LH) y HMG (con actividad semejante a la FSH)
• Administración de FSH y LH: pura, ultrapura o recombinante: El tratamiento se inicia con una dosis de
1000 – 2000 UI de LH IM 3 veces por semana durante varios meses (hasta alcanzar unos valores normales de testosterona); en ese momento se introduce el tratamiento simultáneo con FSH a una dosis de 75 UI IM 3 veces a la semana. Se monitoriza el seminograma hasta lograr recuperar espermatozoides del eyaculado, que se utilizarán para un tratamiento de FIV-ICSI.
• Administración pulsátil de análogos GnRH: se administran pulsos de 1,5 a 10 ng por Kg de peso cada 90-120 minutos mediante la utilización de una bomba de infusión subcutánea. Este tipo de terapia, debido a su complejidad, elevado coste y reducida experiencia, debe reservarse para casos muy seleccionados.
La respuesta al estímulo hormonal va a depender de varios factores, tales como:
• Edad a la que aparece el HH: tienen peor pronóstico las formas congénitas o aquellas que aparecen
antes del desarrollo puberal.
• Volumen testicular en el momento de iniciar el tratamiento hormonal: peor pronóstico cuanto menor sea el volumen testicular.
• Existencia de una criptorquidia asociada, factor de mal pronóstico.
• Concentración basal de inhibina B. Peor pronóstico cuanto menor sea esta concentración
• Severidad del déficit hormonal, peor pronóstico cuanto mayor sea este déficit.
• Índice de masa corporal, con peor pronóstico cuantomayor sea éste.
Después de conseguir el objetivo reproductivo la función sexual puede mejorarse y mantenerse
mediante un tratamiento hormonal sustitutivo con testosterona exógena. La administración de gel de testosterona diario, parches de testosterona o inyecciones logrará restablecer la función sexual, unas erecciones de calidad y una libido normales.
Tratamiento sustitutivo con testosterona
Cuando la prioridad clínica del paciente con hipogonadismo o SDT es el restablecimiento de una función sexual normal o evitar los síntomas del déficit testosterónico se debe usar terapia sustitutiva con testosterona como ha sido expuesto.
El problema es que esto, paradójicamente, puede afectar severamente a su fertilidad, y debe tenerse en cuenta en los pacientes jóvenes o en edad reproductiva.
La administración de testosterona sola suprime la secreción la hipófisis de LH y FSH; y, de hecho, se ha empleado como anticonceptivo masculino. En los años 70 se iniciaron estudios para suprimir la
espermatogénesis con testosterona, aunque no fue hasta los años 90 en que la OMS presentó un
estudio en 4 continentes en el que a voluntarios se les administraron 200 mg de Enantato de Testosterona (ET) IM 1 vez por semana. Un 65% de los varones desarrollaron Azoospermia y el resto Oligozoospermia severa (< de 3millones de esp./ml). El porcentaje de embarazos era similar al conseguido con la utilización de preservativos, pero inferior al ideal. Estos estudios demostraron la eficacia de la testosterona sola como tratamiento anticonceptivo, aunque no todos los varones llegaban a la azoospermia y era precisoidentificar a los no respondedores al tratamiento.
Curiosamente, la respuesta azoospérmica a la terapia con testosterona es diferente en raza asiática
(91%) que en la raza blanca (60%). Y la recuperación de la espermatogénesis tras la supresión del
tratamiento también. Estas diferencias parecen estar relacionadas con ciertos polimorfismos que hacen diferente la respuesta en diferentes razas, siendo más eficaz como anticonceptivo en la asiática. Todo ello hace pensar que sea poco probable que la futura anticoncepción hormonal masculina se base en testosterona sola, al menos en la población occidental.
Se han estudiado una amplia variedad de preparados inyectables de testosterona de acción prolongada. El de mayor duración es el Buciclato de Testosterona con una acción de 3 a 4 meses.
El Undecanoato de testosterona (UT) suprime la espermatogénesis de forma similar al Enantato de
testosterona y puede ser administrado a intervalos de 6 semanas. De hecho, parece que se pueden espaciar más las dosis al proseguir el tratamiento. Gu y colaboradores demostraron en un estudio con 1045 varones fértiles que la inyección mensual de 500mg de UT causa contracepción efectiva, reversible, aceptable y de administración sencilla en varones sanos chinos sin efectos secundarios severos a corto plazo. Ello se logró al disolver el UT oral clásico en aceite de semillas de té. La primera ventaja frente al Enantato de testosterona es obvia a la luz de este estudio, al precisar solo una inyección mensual en vez de semanal. Por otro lado, además resulta ser más seguro, ya que no es hepato-tóxico.
Hace ya unos años que se han incorporado los geles de testosterona al tratamiento del hipogonadismo masculino. Como tratamiento anticonceptivo se ha demostrado la eficacia del gel de testosterona en combinación con un progestágeno inyectable de larga duración, el Acetato de Medroxiprogesterona depot (DMPA), llegando a niveles de Oligospermia y/ò Azoospermia semejantes a los conseguidos mediante la testosterona intramuscular. Cabría por tanto pensar que la administración de gel o de tratamiento por vía tópica de testosterona afectará igualmente a la fertilidad del varón.