Introducción:
Tanto el citrato de clomifeno (CC) como la terapia de remplazo con testosterona (TRT) son tratamientos eficaces para los hombres con hipogonadismo. Buscamos comparar los cambios en los síntomas y la eficacia del tratamiento en hombres hipogonadales antes y después de recibir CC y TRT.
Pacientes y métodos:
52 hombres que recibieron testosterona y 23 hombres que recibieron clomifeno para el hipogonadismo sintomático fueron seguidos prospectivamente por el cambio en los niveles hormonales y los síntomas después del tratamiento. Estos hombres también fueron comparados con hombres eugonadales que no recibieron CC o testosterona durante el mismo período. Se hicieron comparaciones entre los niveles hormonales y los síntomas iniciales y posteriores al tratamiento. Los síntomas fueron evaluados usando los cuestionarios de deficiencia de andrógenos en el envejecimiento masculino (ADAM) y el cuantitativo ADAM (qADAM).
Test de ADAM
- ¿Tiene usted disminución del deseo sexual?
- ¿Tiene falta de energía?
- ¿Sufre disminución de la fuerza y la resistencia,
o ambas? - ¿Ha perdido estatura?
- ¿Ha notado disminución en el disfrute de la vida?
- ¿Está triste o gruñón, o ambos?
- ¿Son sus erecciones menos intensas?
- ¿Ha notado recientemente deterioro en su
capacidad para practicar deportes? - ¿Luego de la cena le da sueño?
- ¿Ha notado recientemente deterioro en
el rendimiento de su trabajo?
Resultados:
La testosterona total en suero aumentó de los niveles previos al tratamiento en todos los hombres (P < 0,05), independientemente del tipo de terapia (TRT: 281-541 ng/dL, CC: 235,5-438 ng/dL). Los hombres que tomaron testosterona reportaron menos síntomas de ADAM después del tratamiento (5-2, P < 0.05). De manera similar, los hombres que tomaban CC reportaron menos síntomas de ADAM después del tratamiento (3.5-1.5, P < 0.05). Por el contrario, los hombres eugonadales tuvieron niveles similares de T (352 vs. 364 ng/dL) y síntomas hipogonadales (1.5 vs. 1.4) antes y después del seguimiento. Cuando evaluamos los síntomas individuales, los hombres tratados con testosterona mostraron aumentos significativos en los resultados de qADAM en la libido, la función eréctil y el rendimiento deportivo. Sin embargo, entre los hombres que recibieron clomifeno, la subpuntuación de qADAM para la libido fue menor después del tratamiento (3.75-3.2, P = 0.04), lo que indica que el clomifeno podría tener un efecto adverso sobre la libido en los hombres hipogonadales.
Conclusiones:
Tanto la testosterona como el clomifeno son medicamentos eficaces para tratar el hipogonadismo; sin embargo, nuestro estudio indica que la testosterona es más eficaz para elevar los niveles de testosterona sérica y mejorar los síntomas hipogonadales. El citrato de clomifeno sigue siendo una modalidad de tratamiento viable para los hombres hipogonadales, pero sus efectos adversos sobre la libido justifican un estudio adicional.
INTRODUCCIÓN
La disminución idiopática de la testosterona relacionada con la edad en hombres adultos es una situación común, que actualmente afecta a cerca del 40% de los hombres adultos de 45 años o más [1]. Los síntomas asociados con la disminución de la testosterona se evalúan a menudo utilizando cuestionarios como el de la deficiencia de andrógenos en el hombre que envejece (ADAM) y el cuantitativo (qADAM). [2,3] La falta de energía, la disfunción eréctil, la disminución de la libido y la disminución de la concentración son síntomas comunes en los hombres con disminución de la testosterona. [4,5,6] Aunque los síntomas son una parte crítica de la definición de hipogonadismo clínicamente relevante, hay una escasez de estudios que evalúen el efecto del tratamiento con testosterona en los síntomas hipogonales.[7]
El citrato de clomifeno (CC) se utiliza frecuentemente fuera de la etiqueta para el tratamiento del hipogonadismo en hombres que desean preservar la función reproductiva [8,9]. El CC es un modulador selectivo de los receptores de estrógeno. Mediante la modulación de los receptores de estrógeno en el hipotálamo y la pituitaria, el citrato de clomifeno antagoniza la retroalimentación negativa del estradiol, mejorando así la liberación de la hormona folículo estimulante (FSH) y la hormona luteinizante (LH). El aumento de la LH eleva posteriormente los niveles séricos de testosterona a través de su acción sobre las células de Leydig en los testículos.[10] El CC puede, en teoría, mejorar los síntomas hipogonadales mientras mantiene los niveles de testosterona hasta 3 años.[11] Como se esperaba, otros estudios han informado que los hombres que reciben CC tuvieron un aumento en los niveles séricos de testosterona, FSH y HL.[12]
En un análisis retrospectivo transversal de edad, hemos demostrado previamente que los hombres que reciben inyecciones de testosterona tenían niveles séricos de testosterona más altos en comparación con los que tomaban CC [11]. No obstante, tanto los hombres que recibían CC como los que recibían inyecciones de testosterona informaron de síntomas hipogonales de base similares. Nuestro análisis transversal no pudo abordar si la suplementación de testosterona y CC mejoraría los síntomas hipogonadales específicos. Por lo tanto, realizamos un estudio de cohorte prospectivo que comparaba los síntomas hipogonadales y la eficacia del tratamiento en hombres que recibían terapia de remplazo con testosterona (TRT) y CC. Se incluyó un grupo de control de hombres eugonadales, que no recibieron TRT ni CC, para mejorar la validez del estudio.
PACIENTES Y MÉTODOS
Tras la aprobación de la Junta de Supervisión Institucional, evaluamos los síntomas hipogonadales utilizando el cuestionario ADAM y qADAM. El cuestionario estándar ADAM consiste en diez preguntas de “sí o no” relativas a los síntomas de la deficiencia de andrógenos (rango 0-10). El cuestionario de la qADAM se basa en el cuestionario “ADAM” utilizando las mismas diez preguntas con igual valoración que el documento original, pero utiliza una escala de Likert de 1-5 para cuantificar cada respuesta en lugar de una respuesta de “sí” o “no”. Mediante la cuantificación, se puede evaluar la magnitud de determinados síntomas. Las puntuaciones del cuestionario “ADAM” oscilan entre 10 y 50, y las puntuaciones más altas indican síntomas hipogonadales menos graves; sin embargo, no hay una puntuación concreta que permita diagnosticar con precisión el hipogonadismo.
Nuestro grupo de estudio incluyó 52 hombres con TRT y 23 hombres con CC. Todos los hombres tenían dos valores separados de testosterona total en suero temprano en la mañana <300 ng/dL asociados con ≥3 síntomas hipogonadales verificados en el cuestionario ADAM. Los hombres que se quejaron de infertilidad fueron excluidos porque el tratamiento de fertilidad por sí solo podría perjudicar la libido y la función eréctil. También excluimos a los hombres con hipogonadismo secundario (con LH y FSH por debajo del normal). Los hombres recibieron CC si querían preservar la fertilidad durante el tratamiento de los síntomas de hipogonadismo. El objetivo de la terapia era la mejora de los síntomas en lugar de un nivel umbral de testosterona.
Durante el mismo período de estudio, 52 hombres eugonadales que no recibían testosterona o CC fueron incluidos como grupo de control para la comparación. Estos hombres se sometieron a una estimación hormonal y fueron tratados por condiciones urológicas benignas como la disfunción eréctil y los síntomas del tracto urinario inferior. Estos hombres eugonadales no estaban recibiendo testosterona o CC.
De los hombres con testosterona, 27 recibieron inyecciones de testosterona y 25 hombres recibieron gel de testosterona. Anteriormente reportamos los niveles hormonales y los síntomas (cuestionario ADAM solamente) en los 52 hombres que recibieron TST.[7] Reportamos los sub puntajes individuales en el cuestionario de qADAM en los hombres que recibieron TST en este estudio y los comparamos con los hombres que recibieron CC durante el mismo período.
La eficacia del tratamiento se evaluó comparando los niveles de testosterona sérica antes y después del tratamiento. Los valores previos y posteriores al tratamiento se determinaron en la misma visita en que se completaron los cuestionarios ADAM y qADAM. La testosterona y el estradiol se midieron por radioinmunoanálisis utilizando el sistema de inmunoanálisis Access® 2. Dado que se conoce la variabilidad temporal de la concentración de testosterona sérica en los hombres que reciben inyecciones de testosterona, las muestras se recogieron durante la visita de seguimiento programada del paciente sin preocuparse especialmente por el momento de la última inyección. La variabilidad de los niveles se obvió por la naturaleza aleatoria del sorteo y el número de pacientes encuestados. Los datos se analizaron utilizando Excel® e IBM SPSS (IBM SPSS Statistics 21, Armonk, NY, EE.UU.). Todos los valores se muestran como la media ± desviación estándar. La prueba de Mann-Whitney se utilizó para evaluar las diferencias entre los grupos con P ≤ 0,05 considerado estadísticamente significativo.
RESULTADOS
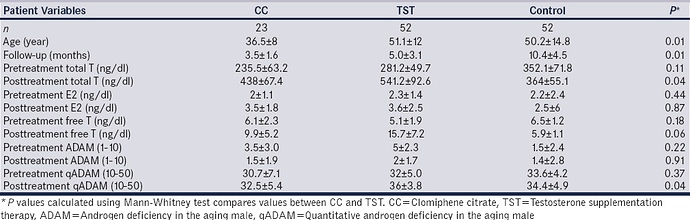
Los hombres recibiendo CC eran más jóvenes que los que recibían TST (36 vs. 51, P = 0.01). Los niveles de testosterona aumentaron en los hombres que recibieron CC y TST (CC: 235-438 ng/dL, P < 0,05; TST: 231-541 ng/dL, P < 0,05). Como era de esperar, los hombres que recibieron TST tuvieron un mayor y significativo aumento (delta) en el promedio de testosterona sérica (310 ng/dL) en comparación con los hombres que recibieron CC (233 ng/dL, P = 0,04). Sin embargo, el cambio en los niveles de estradiol fue similar entre los hombres que recibieron CC y los hombres que recibieron TST (3,5 ng/dL vs. 3,6 ng/dL, P = 0,87).
Ambas cohortes que recibieron CC y TST tuvieron mejoras en los síntomas hipogonadales usando el cuestionario ADAM (CC: 3.5 vs. 1.5; TST: 5.0 vs. 2.0, P < 0.05) y el cuestionario qADAM (CC: 30.7-32.5; TST: 32-36, P < 0.05). Mientras que tanto los hombres en CC como en TST tuvieron mejoras en los síntomas hipogonadales, los hombres en TST experimentaron una mayor resolución de los síntomas según la medición de qADAM [Tabla 1]. Este aumento en la qADAM indica que los pacientes en TST mostraron una mejora cuantificable significativa en los síntomas y experimentaron síntomas hipogonadales menos severos que los hombres que tomaban CC. Por el contrario, los hombres eugonadales tuvieron niveles similares de TST (352 vs. 364 ng/dL) y síntomas hipogonadales (1,5 vs. 1,4) antes y después del seguimiento.
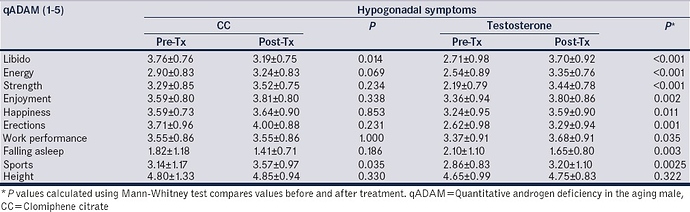
Cuando evaluamos los síntomas individuales, los hombres tratados con TST mostraron aumentos significativos en las puntuaciones de qADAM en la libido (2,74-3,70, P ≤ 0,001), la energía (2,54-3,35, P ≤ 0,001), la fuerza (2,19-3,44, P ≤ 0,001), el disfrutar (3,36-3. 80, P ≤ 0,001), felicidad general (3,24-3,59, P = 0,011), función eréctil (2,62-3,29, P = 0,001), rendimiento laboral (3,37-3,68, P = 0,035), tendencia a dormirse (2,10-1,65, P = 0,003) y rendimiento deportivo (2,86-3,20, P = 0,025). No hubo diferencias en las puntuaciones de qADAM entre las diferentes modalidades de TST. Los pacientes que recibieron CC sólo mostraron un beneficio significativo con respecto al rendimiento deportivo (3,14-3,57, P = 0,035). Notablemente, entre los hombres que recibieron CC, la subpuntuación de qADAM para la libido fue menor después del tratamiento (3.75-3.2, P = 0.04), lo que indica que el CC podría tener un efecto adverso sobre la libido en hombres hipogonadales. Ninguna otra subpuntuación en la qADAM demostró un cambio significativo en los hombres que recibieron CC [Tabla 2].
DISCUSIÓN
Nuestro estudio sobre los efectos de la TST y el CC en los resultados de los pacientes (niveles hormonales y síntomas) ha confirmado que tanto la TST como el CC son eficaces en el tratamiento del hipogonadismo; sin embargo, la magnitud del efecto del tratamiento observado en los varones que recibieron la TST fue mejor. Nuestro análisis demostró que los pacientes que recibieron TST lograron mayores aumentos en la testosterona sérica y una mejor resolución de los síntomas (mayores puntuaciones en la qADAM) en comparación con los que fueron tratados con CC. En un análisis más detallado de las subpuntuaciones de qADAM, nuestro estudio describió aumentos significativos en todas las categorías evaluadas, aparte de la altura, después del tratamiento con TST, mientras que los hombres que recibieron tratamiento con CC informaron de una mejora en la capacidad deportiva pero una peor libido.
La asociación entre los síntomas hipogonadales y los niveles séricos de testosterona ha sido bien documentada. La investigación previa del grupo de Estudio Europeo del Envejecimiento Masculino delineó una correlación inversa significativa entre los niveles séricos de testosterona y la presencia de erecciones matinales deficientes, bajo deseo sexual y disfunción eréctil.[6] Una reciente investigación retrospectiva muestra que los pacientes tratados con TST o CC informaron de síntomas hipogonadales similares; en promedio, los pacientes que recibieron CC, inyecciones de testosterona y geles, informaron de una qADAM total de 35, 39 y 36, respectivamente.[11]
Los resultados de este presente estudio muestran que, aunque los pacientes a los que se les prescribió CC tuvieron un aumento en la puntuación general de qADAM, los pacientes informaron de una disminución significativa de la libido. La etiología de este efecto de CC en la libido no ha sido completamente dilucidada, pero se teoriza que la modulación del receptor de estrógeno podría tener efectos negativos en la libido. El estrógeno, a pesar de que se considera ampliamente una hormona “femenina”, sigue siendo importante para mantener la libido en los hombres [13]. Sin embargo, la modulación del receptor de estrógeno por el CC puede perjudicar la acción del estrógeno y, por consiguiente, causar un deterioro del impulso sexual [13]. Aunque el CC es eficaz para mejorar los síntomas hipogonadales generales, el CC en este estudio parece afectar negativamente a la libido. Se necesitan estudios más amplios para validar el efecto del CC en la libido.
Aunque se creó un diseño de estudio prospectivo para explorar las sutiles diferencias de la terapia hipogonadal, el estudio tiene algunas limitaciones. La primera limitación que se debe abordar es la potencial ambigüedad con respecto al impulso de la terapia con CC. Los hombres que utilizaron CC eran más jóvenes, reportaron mayores puntuaciones de libido antes del tratamiento y utilizaron CC para ayudar tanto con el hipogonadismo como para preservar la fertilidad en lugar de tratar los síntomas hipogonadales solos, creando así una desconexión entre la lógica del tratamiento de TST versus CC. No obstante, los hombres con infertilidad y baja testosterona parecen reportar síntomas hipogonadales similares a los hombres sin infertilidad [14] Los cuestionarios ADAM y qADAM son validados para la comparación transversal de los síntomas de la testosterona sérica y la hipogonadal. Dado que no hay cuestionarios validados universalmente para estudiar el cambio en los síntomas hipogonadales, utilizamos los cuestionarios ADAM y qADAM que se usan comúnmente y son fáciles de administrar en la clínica.[15] Dada la naturaleza no paramétrica de los datos, el análisis de potencia habría sido difícil de realizar y potencialmente inexacto debido a la dependencia de la simulación de datos; sin embargo, la utilidad de este análisis es evidente y se incorporará en el análisis posterior. Otra limitación y desafío de este estudio fue la falta de un cálculo de potencia a priori. Sin embargo, anticipamos que estos datos servirán como referencia para determinar el tamaño de la muestra en futuros trabajos de comparación de la TST y el CC para los síntomas hipogonadales. La prueba de hipótesis múltiples no se realizó en este momento debido a la naturaleza generadora de hipótesis del estudio.
El tamaño de la muestra de pacientes no es grande, a menudo es secundario a la intención de los pacientes, ya que los pacientes que no desean preservar la fertilidad tienden a preferir la terapia por TST ya que no están tan familiarizados con el CC. El estudio utiliza una asignación 2:1 y aunque no es ideal, es aceptable dada la naturaleza del estudio.
Los síntomas hipogonadales son subjetivos, lo que puede complicar el diagnóstico del paciente e identificar el éxito del tratamiento. Un factor de confusión es que la satisfacción del paciente puede variar en función de las percepciones psicológicas sobre los posibles beneficios conferidos por la terapia. Las percepciones sobre el tipo de terapia prescrita también podrían haber influido en las expectativas del paciente. Los resultados también podrían haberse visto afectados por comorbilidades médicas preexistentes, ya que estas variables no se incluyeron explícitamente en el análisis. La diferencia entre los tiempos de seguimiento es diferente y puede sugerir diferencias en la satisfacción de los pacientes entre las dos terapias, aunque esta interpretación no fue explorada en este estudio actual. Debido a que existe un gran número de hombres jóvenes, que presentan síntomas hipogonadales pero necesitan preservar la fertilidad, una mejor comprensión sobre el beneficio o la falta de éste para las opciones de tratamiento alternativo será importante cuando se proporcionen y discutan las opciones de tratamiento para esta población.
CONCLUSIONES
Tanto la testosterona como el clomifeno son medicamentos eficaces para tratar el hipogonadismo; sin embargo, nuestro estudio indica que la TST es más eficaz para elevar los niveles de testosterona sérica y mejorar los síntomas del hipogonadismo. El CC sigue siendo una modalidad de tratamiento viable, pero su efecto adverso sobre la libido merece un estudio más profundo.
CC - citrato de clomifeno
TST - testosterona
TRT - terapia de remplazo de testosterona
Referencias y Bibliografia
Footnotes
Financial support and sponsorship: Nil.
Conflicts of interest: There are no conflicts of interest.
REFERENCES
PMCID: PMC5508437
PMID: 28717276
Indian J Urol. 2017 Jul-Sep; 33(3): 236–240.
Testosterone versus clomiphene citrate in managing symptoms of hypogonadism in men
Pranav Dadhich,* Ranjith Ramasamy,1 Jason Scovell, Nathan Wilken, and Larry Lipshultz
-
Mulligan T, Frick MF, Zuraw QC, Stemhagen A, McWhirter C. Prevalence of hypogonadism in males aged at least 45 years: The HIM study. Int J Clin Pract. 2006;60:762–9. [PMC free article] [PubMed] [Google Scholar]
-
Morley JE, Charlton E, Patrick P, Kaiser FE, Cadeau P, McCready D, et al. Validation of a screening questionnaire for androgen deficiency in aging males. Metabolism. 2000;49:1239–42. [PubMed] [Google Scholar]
-
Mohamed O, Freundlich RE, Dakik HK, Grober ED, Najari B, Lipshultz LI, et al. The quantitative ADAM questionnaire: A new tool in quantifying the severity of hypogonadism. Int J Impot Res. 2010;22:20–4. [PMC free article] [PubMed] [Google Scholar]
-
Bhasin S, Cunningham GR, Hayes FJ, Matsumoto AM, Snyder PJ, Swerdloff RS, et al. Testosterone therapy in adult men with androgen deficiency syndromes: An endocrine society clinical practice guideline. J Clin Endocrinol Metab. 2006;91:1995–2010. [PubMed] [Google Scholar]
-
Traish AM, Miner MM, Morgentaler A, Zitzmann M. Testosterone deficiency. Am J Med. 2011;124:578–87. [PubMed] [Google Scholar]
-
Wu FC, Tajar A, Beynon JM, Pye SR, Silman AJ, Finn JD, et al. Identification of late-onset hypogonadism in middle-aged and elderly men. N Engl J Med. 2010;363:123–35. [PubMed] [Google Scholar]
-
Ramasamy R, Wilken N, Scovell JM, Lipshultz LI. Effect of testosterone supplementation on symptoms in men with hypogonadism. Eur Urol. 2015;67:176–7. [PubMed] [Google Scholar]
-
Willets AE, Corbo JM, Brown JN. Clomiphene for the treatment of male infertility. Reprod Sci. 2013;20:739–44. [PubMed] [Google Scholar]
-
Moskovic DJ, Katz DJ, Akhavan A, Park K, Mulhall JP. Clomiphene citrate is safe and effective for long-term management of hypogonadism. BJU Int. 2012;110:1524–8. [PubMed] [Google Scholar]
-
Goldstein SR, Siddhanti S, Ciaccia AV, Plouffe L., Jr A pharmacological review of selective oestrogen receptor modulators. Hum Reprod Update. 2000;6:212–24. [PubMed] [Google Scholar]
-
Ramasamy R, Scovell JM, Kovac JR, Lipshultz LI. Testosterone supplementation versus clomiphene citrate for hypogonadism: An age matched comparison of satisfaction and efficacy. J Urol. 2014;192:875–9. [PubMed] [Google Scholar]
-
Katz DJ, Nabulsi O, Tal R, Mulhall JP. Outcomes of clomiphene citrate treatment in young hypogonadal men. BJU Int. 2012;110:573–8. [PubMed] [Google Scholar]
-
Finkelstein JS, Yu EW, Burnett-Bowie SA. Gonadal steroids and body composition, strength, and sexual function in men. N Engl J Med. 2013;369:2457. [PubMed] [Google Scholar]
-
Satkunasivam R, Ordon M, Hu B, Mullen B, Lo K, Grober E, et al. Hormone abnormalities are not related to the erectile dysfunction and decreased libido found in many men with infertility. Fertil Steril. 2014;101:1594–8. [PubMed] [Google Scholar]
-
Bernie AM, Scovell JM, Ramasamy R. Comparison of questionnaires used for screening and symptom identification in hypogonadal men. Aging Male. 2014;17:195–8. [PubMed] [Google Scholar]



 pero vamos reconozco, que en los demás alegre lo que se dice alegre como un chaval pues no
pero vamos reconozco, que en los demás alegre lo que se dice alegre como un chaval pues no 


