¿Qué es un péptido?
Los péptidos (proteínas) están presentes en todas las células vivas y poseen una variedad de actividades bioquímicas. Algunos péptidos se sintetizan en los ribosomas de una célula mediante la traducción del mRNA (RNA mensajero) en hormonas y moléculas de señalización, por ejemplo. Otros péptidos se ensamblan (en lugar de ser sintetizada) y se convierten en enzimas con una amplia variedad de funciones. Los péptidos también constituyen la estructura de los receptores que esperan la unión de las hormonas y las moléculas de señalización.
Un péptido es una molécula creada por la unión de dos o más aminoácidos. En general, si el número de aminoácidos es menor a cincuenta, estas moléculas se denominan péptidos, mientras que las secuencias más grandes se conocen como proteínas.
Así que los péptidos pueden ser considerados como proteínas pequeñas. Ellos no son más que cadenas de aminoácidos.
Los constituyentes primos de los péptidos (aminoácidos)
Los aminoácidos son pequeñas moléculas compuestas por átomos. Como parte de su estructura, poseen una agrupación de un nitrógeno (N) un átomo de hidrógeno unido a dos átomos (H). Esto se llama un grupo amino y se escribe como (NH2). Además, su estructura también se compone de una segunda agrupación de carbono (C) unido a dos átomos de oxígeno (O) y un átomo de hidrógeno. Este grupo se llama “grupo carboxilo” y se escribe como (COOH).
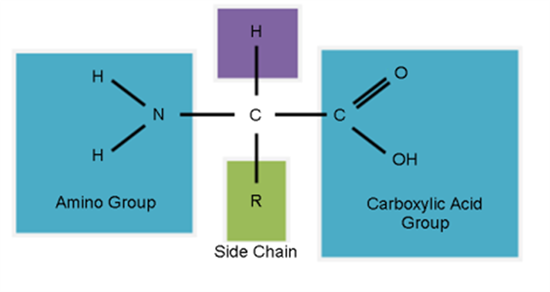
Entre estos dos grupos hay átomos y enlaces únicos para cada aminoácido. En otras palabras, todos los aminoácidos poseen las dos agrupaciones (amino y carboxilo) como puntos finales entre las que se intercalan un conjunto único de átomos.
Aminoácidos
En el interior del cuerpo humano hay veinte aminoácidos normales, utilizados por las células en la biosíntesis del péptido (es decir, la creación celular de péptidos procedente de los aminoácidos). Nuestro código genético especifica cómo sintetizar péptidos y proteínas a partir de estos aminoácidos.
Los aminoácidos se clasifican en dos grupos: los aminoácidos esenciales y aminoácidos no esenciales.
Un aminoácido esencial es un aminoácido indispensable que no puede ser producido por el cuerpo y deben ser suministrados por los alimentos. Estos incluyen: isoleucina, leucina, lisina, metionina, fenilalanina, treonina, triptófano y valina. Otro aminoácido - histidina se considera semi-esencial porque el cuerpo no siempre requiere fuentes dietéticas de esta.
Los aminoácidos no esenciales son producidos por el cuerpo a partir de los aminoácidos esenciales o de la descomposición habitual de proteínas. Los aminoácidos no esenciales son: arginina, alanina, asparagina, ácido aspártico, cisteína, glutamina, ácido glutámico, glicina, prolina, serina y tirosina.
Todos los veinte aminoácidos son igual de importantes a la hora de mantener un cuerpo sano. Ellos son los constituyentes primos de los péptidos y las proteínas.
Las abreviaturas estándar para los aminoácidos son de dos tipos: una forma compuesta por una letra y la otra por tres letras. Estas son:
A - Ala - alanina
C - Cys - Cisteína
D - Asp - Ácido aspártico
E - Glu - Ácido glutámico
F - Phe - fenilalanina
G - Gly - Glicina
H - Su - Histidina
I - Ile - Isoleucina
K - Lys - Lisina
L - Leu - La leucina
M - Met - Metionina
N - Asn - asparagina
P - Pro - Proline
Q - Gln - Glutamina
R - Arg - Arginina
S - Ser - Serina
T - Thr - Treonina
V - Val - Valina
W - Trp - Triptófano
Y - Tyr - Tirosina
Existen aminoácidos ya sea en el formato D (dextro) o en formato L (levo). La mayoría de los aminoácidos que se encuentran en la naturaleza (y todo dentro de las células humanas) son de la forma L. Generalmente todos los aminoácidos excepto la glicina tienen una imagen semejante a la forma L. Esta imagen similar se llama la forma D. Es común hacer referencia a la forma L- (formato natural) para dejar fuera la denominación “L”, mientras que la designación “D” se escribe siempre de forma explícita.
Los aminoácidos D- se encuentran naturalmente en las paredes celulares bacterianas y son utilizados en algunos péptidos sintéticos para hacer un péptido más estable o más resistentes a la degradación.
Aminoácido + Aminoácido = Péptido
Los aminoácidos se unen entre sí, esto se le conoce como un “enlace peptídico”. Un “enlace peptídico” es una unión en la que el átomo de nitrógeno de un aminoácido (desde el grupo amino (NH2)) se une al átomo de carbono del grupo carboxilo de otro aminoácido (COOH).
Durante este proceso de unión se libera una molécula de agua. Esto se llama reacción de condensación.
El enlace CO-NH resultante se le llama enlace peptídico, y la molécula resultante se le llama amida.
En la siguiente nota de imagen, el grupo COOH cede un enlace de hidrógeno de oxígeno (OH) y el grupo NH2 da un hidrógeno (H). Esto forma H2O, que es una molécula de agua que no es parte del péptido ya recién creado.

Esta reacción crea un enlace peptídico entre dos aminoácidos creando así un péptido. Podemos llamar a este péptido un dipéptido (compuesto por dos aminoácidos).
Este proceso se puede repetir utilizando los veinte aminoácidos como materia prima para crear cadenas de péptidos más largas. A veces las cadenas de péptidos constan de 50 a 100 aminoácidos, estas se denominan polipéptidos. A menudo, una cadena peptídica más allá de 100 aminoácidos se la denomina como proteína.
GHRP-6 es un péptido compuesto por sólo seis aminoácidos. Su estructura se escribe a menudo como Su-DTrp-Ala-Trp-DPhe-Lys-NH2
Tenga en cuenta que la agrupación de carboxilo (COOH) se la da por hecho estar en la primera posición y por eso no está escrito. El grupo amino (NH2) es escrito en la última posición. La “carne” o la parte que hace al GHRP-6 distinto es la secuencia que hay en medio de la unión entre la histidina y la forma “D” de triptófano unido a alanina unido a triptófano unido a la forma "D” de la fenilalanina unida a la lisina.
La unificación de los péptidos está formada por agua (H2O) de condensación (eliminación de agua). Lo opuesto también es válido. Un enlace peptídico puede ser degradado por hidrólisis (adición de agua).
Las Estructuras de aminoácidos de los péptidos se analizan en este hilo
Péptidos liberadores de la hormona del crecimiento (GHRP) (iniciadores de pulsos de GH):
-
GHRP-6 (Su-DTrp-Ala-Trp-DPhe-Lys-NH2)
-
GHRP-2 (DAla-D-2-Nal-Ala-Trp-Lys-DPhe-NH2)
-
Hexarelina (Su-D-2-metil-Trp-Ala-Trp-Lys-DPhe-NH2)
-
Ipamorelin (Aib-His-D-2-Nal-DPhe-Lys-NH2) - Ref-1
NOTAS:
Aib = Ácido Aminoisobutyryco
D-2-Nal = forma “D” de 2’-naftilalanina
Hormona liberadora de la hormona del crecimiento ([COLOR=“#008000”]GHRH[/COLOR]) (amplifica el impulso iniciado de GHRP):
-
Hormona liberadora de la hormona del crecimiento (GHRH) aka (alias) GRF (1-44) (Tyr-Ala-Asp-Ala-Ile-Phe-Thr-Asn-Ser-Tyr-Arg-Lys-Val-Leu-Gly-Gln-Leu-Ser-Ala-Arg-Lys-Leu-Leu-Gln-Asp-Ile-Met-Ser-Arg-Gln-Gln-Gly-Glu-Ser-Asn-Gln-Glu-Arg-Gly-Ala-Arg-Ala-Arg-Leu-NH2) = La vida media es menor a 10 minuto, tal vez tan solo de 5 minutos. - Ref-2
-
GRF (1-29) aka Sermorelin (Tyr-Ala-Asp-Ala-Ile-Phe-Thr-Asn-Ser-Tyr-Arg-Lys-Val-Leu-Gly-Gln-Leu-Ser-Ala-Arg-Lys-Leu-Leu-Gln-Asp-Ile-Met-Ser-Arg-NH2) - La porción biológicamente activa de los 44 aminoácidos de GHRH = a vida media de “menor a 10 minutos”, tal vez tan sólo 5 minutos. - Ref-3
-
Análogos de GRF de mayor duración B[/B]:
-
Sustituir el segundo aminoácido alanina con D-alanina sólo para modificar GRF (1-29), D-Ala2 GRF (1-29) (Tyr-DAla-Asp-Ala-Ile-Phe-Thr-Asn-Ser-Tyr-Arg-Lys-Val-Leu-Gly-Gln-Leu-Ser-Ala-Arg-Lys-Leu-Leu-Gln-Asp-Ile-Met-Ser-Arg-NH2) = Vida media “cerca de 10 minutos” - Ref-4
-
Sustituir el segundo, octavo, décimo quinto y el vigésimo séptimo amino ácido y quedar modificado GRF (1-29) o CJC-1295 sin una lisina añadida y sin DAC (es decir, la parte que se unirá a la albúmina y que la vida media sea de días) (Tyr-DAla-Asp-Ala-Ile-Phe-Thr-Gln-Ser-Tyr-Arg-Lys-Val-Leu-Ala-Gln-Leu-Ser-Ala-Arg-Lys-Leu-Leu-Gln-Asp-Ile-Leu-Ser-Arg-NH2) = Vida media de al menos 30 minutos, más o menos - Ref-5
-
CJC-1295 (Tyr-DAla-Asp-Ala-Ile-Phe-Thr-Gln-Ser-Tyr-Arg-Lys-Val-Leu-Ala-Gln-Leu-Ser-Ala-Arg-Lys-Leu-Leu-Gln-Asp-Ile-Leu-Ser-Arg-Lys-(Maleimidopropionyl)-NH2) = La vida media se mide en días, - Ref-6
NOTAS:
Lys = enlazador a la afinidad de drogas complejas (alias (Maleimidopropionyl))
“Desde que la GH se libera de una manera pulsátil y se observa un mayor nivel de GH entre 15 y 30 min después de la administración subcutánea de análogos de GH-RH, la hidrólisis hecha por las enzimas de tipo tripsina no podría afectar el resultado de la estimulación.” - Análogo de la potente y resistente tripsina de la hGH-RH, JAN IZDEBSKI, J. Peptide Sci. 10: 524–529 (2004)
El análogo que se encuentra el estudio citado anteriormente resistió la degradación durante 30 minutos. La cita implica que si su análogo puede durar 30 minutos es porque se ha aprovechado el potencial de un solo pulso.
Desde otro pulso no se generará hasta aproximadamente 2,5 - 3 horas, los análogos que duran más de 30 minutos hasta 3 horas no son más beneficiosos.